Anorgaaniline Keemia/Sümmeetria
Antud peatükis toetutakse raamatule Chemical Structure and Reactivity.[1]
Molekulide omaduste ja struktuuri vahel saab leida seoseid kasutades selle mõistmiseks molekuli sümmeetriaomadusi. Näiteks saab hinnata, millised molekulis olevatest aatomitest käituvad ekvivalentselt, kas molekul on kiraalne või mitte, kas molekulil on dipoolmoment või mitte. Need omadused sõltuvad aatomite paigutusest molekulis ning seda saab efektselt kirjeldada sümmeetria abil.
Lisaks saab molekuli sümmeetriaelementide abil ennustada tema spektroskoopilisi omadusi. Kvantmehaaniliste arvutuste jaoks kasutatavad kanoonilised orbitaalid saadakse sümmeetria abil.
Sümmeetriaelemendid ja -teisendused
[muuda]Molekuli sümmeetriaomadusi kirjeldatakse kindlate sümmeetriaelementide abil ning need saadakse, kui läbi viia mingile sümmeetriaelemendile vastav sümmeetriateisendus. Sümmeetriateisendus on mingi tegevus, mis annab molekuli samal kujul tagasi. Sümmeetriaelemendid on identsus E, inversioonitsenter i, pöördtelg Cn, peegeltasand σ, peegelpöördtelg Sn.
Identsus E
[muuda]Identsusele E vastav sümmeetriateisendus tähendab seda, et molekul ei liigu. Ehk kui mitte midagi teha, siis saame identsuse. Identsus on kõikidel molekulidel olemas. Analoogselt matemaatikas numbriga 0 võib mõelda, et identsus on sümmeetriaelementide '0'.
Inversioonitsenter i
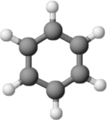
[muuda]Inversioonitsentrile i vastav sümmeetriateisendus on inversioon läbi mingi punkti. Inversiooni käigus molekuli iga aatom viiakse mingi punkti suhtes teisele poole täpselt samale kaugusele. Kui toetuda Cartesiuse koordinaatide peale ning ette kujutada, et mingil molekuli aatomil on (x, y, x) koordinaadid ning inversioonitsentri koordinaat on (0, 0, 0), siis pärast inversiooni tema koordinaadid on (-x, -y, -z). Kui aatomite paigutus pärast inversiooni annab meile molekuli samal kujul tagasi, on tal inversioonitsenter olemas. Näiteks inversioonitsenter on benseenil, heksafluroväävlil ja trans-1,2-dikloroetüleenil, kuid mitte cis-1,2-dikloroetüleenil.
-
Benseen
-
SF6
-
trans-1,2-dikloroetüleen
-
Puudub inversioonitsenter, võrdle trans-1,2,-dikloroetüleeniga
Pöördtelg Cn
[muuda]Pöördteljele Cn vastav sümmeetriateisendus tähendab seda, et molekulis toimub ümber pöördtelje pöördtelje 360/n kraadi võrra (n = 1,2,3,4,6 ehk pöörlemine vastavalt 360, 180, 120, 90 või 60 kraadi võrra). Kui pöörlemine annab molekuli samal kujul tagasi, on tal olemas vastav pöördtelg Cn. On ilmselge, et kõikidel molekulides on olemas pöördtelg C1, mis on sama identsusele vastavale sümmeetriaoperatsioonile. Lisaks, kokkuleppeliselt määratakse molekulile põhitelg, mis vastab tema kõrgeima väärtusega pöördteljele Cn ning see vastab z-teljele Cartesiuse koordinaatsüsteemis. Näitena on toodud benseeni pöördteljed.

Peegeltasand ehk sümmeetriatasand σ
[muuda]peegeltasandile σ vastav sümmeetriateisendus tähendab seda, et molekuli aatomid peegeldatakse mingi tasandi suhtes teisele poole. Kui molekulil on mitu peegeltasandit, siis eristatakse alaindeksiga horisontaalseid ja vertikaalseid peegeltasandeid. Horistontaalne peegeltasand tähistatakse σh. Lisaks, σd viitab sidemeid lõikavale peegeltasandile ning σv aatomeid läbivale peegeltasandile. Näiteks benseenil on kokku 6 peegeltasandit.

Peegelpöördtelg Sn
[muuda]Peegelpöördteljele Sn vastav sümmeetriateisendus tähendab sisuliselt kahte järjestikust tegevust - esiteks pöörlemine ümber peegelpöördtelje Sn mingi nurga võrra (analoogselt pöördteljele Cn) ning sellele järgnevat peegeldust läbi tasandi, mis läbib peegelpöördtelge Sn ja on risti sellega. Kusjuures, molekulil ei pea olema pöördtelge ega peegeltasandit, et tal peegelpöördtelg olemas oleks. Lisaks, Esimest järku peegelpöördtelg on samane peegeltasandile ning teist järku peegepöördtasand on samane inversioonitsentrile ehk S1 = σ ning S2 = i. Näitena on toodud ferrotseen.

Loetletud sümmeetriaoperatsioone saab ka endale selgeks teha ka veebileheküljel symotter.org.
Punktigrupid
[muuda]Kindlad sümmeetriaelementide koosseisud kategoriseeritakse punktigruppi ning igat molekuli saab määrata kindlasse punktigruppi. Punktigrupp kirjeldab efektselt molekuli sümmeetriat.
Allpool toodud tabelis on toodud erinevad punktigrupid, nendele vastavad sümmeetriaelemendid ning punktigruppi kuuluvatest molekulidest.
Paremal pool on toodud skeem, mida saab kasutada, et määrata millisesse punktigruppi mingi molekul kuulub.

Sümmeetriaelementide rakendused
[muuda]Ekvivalentsete aatomite määramine molekulis
[muuda]Sümmeetriaoperatsioonidega saab määrata, millised aatomid on molekulis ekvivalentsed. Molekulis on aatomid ekvivalentsed siis, kui nad kattuvad üksteisega molekuli sümmeetriaoperatsioonide käigus. PF5 molekulis ei ole kõik fluorid ekvivalentsed. 3 fluori aatomit asuvad samal molekuli horisontaalsel peegeltasandil, kuid 2 fluori, mis asuvad pöördteljel C3, eristuvad nendest, kuna molekuli sümmeetriaoperatsioonide käigus nad ei saa kattuda horisontaalsel peegeltasandil asuvate fluori aatomitega.
-
Vertikaalsed fluori aatomid ja horisontaalsed fluori aatomid erinevad üksteisest.
Kiraalsus
[muuda]Kiraalsel molekulil on kaks enantiomeeri ehk kaks isomeeri, mis on üksteise peegelpildid. Selgub, et kui molekulil puudub mistahes peegelpöördtelg Sn, siis ta ei saa olla kiraalne. Tasub meelde tuletada, et S1 = σ ning S2 = i. Seega kui molekulis on peegeltasand või inversioonitsenter, siis ta ei ole kiraalne.
Dipoolmomendi määramine
[muuda]Dipoolmoment on molekuli omadus. Seega ei tohi sümmeetriateisendused seda muuta. Dipoolmomendi suund ei tohi olla risti ei pöördtelje (dipoolmomendi suund muutub 360/n kraadi võrra) ega peegeltasandiga (dipoolmomendi suund pöörab 180 kraadi võrra). Lisaks, kui molekulil on inversioonitsenter, siis tal ei saa olla dipoolmomenti.
Sümmeetria ja orbitaalid
[muuda]Molekulis saab orbitaale jagada kas sümmeetrilisteks või antisümmeetrilisteks vastavalt orbitaali käitumisele kindla sümmeetriateisenduse suhtes. Antud ideed saab illustreerida matemaatikas kasutatavate mõistete paaritu ja paarisfunktsioon[1]. Paarisfunktsioon on funktsioon, mille väärtus jääb samaks, kui selle muutuja väärtus muuta vastupidiseks. Näiteks cos(x) on paarisfunktsioon, sest cos(x0) = cos(-x0). sin(x) on aga paaritu funktsioon, sest sin(x0) = -sin(-x0).
Aatomorbitaale saab jagada sümmeetrilisteks või antisümmeetrilisteks näiteks aatomit läbiva peegeltasandi peegeldamise või aatomi keskpunkti inversiooni suhtes. H2O molekulis saab orbitaale eristada peegeldamise suhtes vertikaaltasandil yz. Orbitaali saab jagada kas sümmeetriliseks, kui tema väärtus jääb pärast peegeldamist samaks, või antisümmeetriliseks, kui tema väärtus muutub vastupidiseks. Sümmeetrilist orbitaali tähistatakse alaindeksiga g (gerade, saksa keeles paaris-, nt paarisarv) ja antisümmeetrilist orbitaali alaindeksiga u (ungerade, saksa keeles paaritu, nt paaritu arv).
MO-teoorias (molekulaarorbitaalid) arvestatakse molekulorbitaalide sümmeetriat nende iseloomustamisel ja eristamisel. Tavaliselt tehakse seda kahte sidet omava aatomi keskpunkti suhtes. Kui inversioonil molekulorbitaali märk muutub, siis nimetatakse orbitaali antisümmeetriliseks ehk ungerade. Kui pöörlemisel märk ei muutu, siis sümmeetriliseks ehk gerade. Kovalentsete sidemete puhul on siduvad σ-orbitaalid ja antisiduvad π*-orbitaalid gerade-sümmeetriaga. Siduvad π-orbitaalid ja antisiduvad σ*-orbitaalid ungerade-sümmeetriaga.
Viited
[muuda]- ↑ Keeler, James.; Wothers, Peter. (2014). Chemical Structure and Reactivity: An Integrated Approach. Oxford University Press. p.79-97